Αυτοσωματική Επικρατούσα Πολυκυστική Νόσος των Νεφρών
Οι κύστεις των νεφρών είναι κοιλότητες – σάκοι περιστοιχισμένες από ένα επιθήλιο γεμάτες με υγρό ή ημιστερεό υλικό και οι οποίες προέρχονται από τα νεφρικά σωληνάρια. Μετά την επίτευξη ενός μεγέθους, ίσως μερικών χιλιοστών, οι περισσότερες κύστεις χάνουν την επαφή τους με το σωληνάριο και αποκόπτονται. Η βλαπτική επίδραση των κύστεων εξαρτάται κυρίως από το μέγεθός, τη θέση τους και τελικά την απώλεια της υπερδιήθησης, ως αντιρροπιστικός μηχανισμός, των υπαρχόντων νεφρώνων.
Συχνότητα Εμφάνισης της ADPKD

Πως κληρονομείται η ADPKD
Η Αυτοσωματική Επικρατούσα Πολυκυστική Νόσος των Νεφρών (ADPKD) είναι πάθηση που κληρονομείται με τον αυτοσωμικό επικρατούντα χαρακτήρα, με 100% διεισδυτικότητα (όσο αφορά τις νεφρικές κύστεις), αλλά με μεγάλη ποικιλομορφία στην έκφραση και τις κλινικές εκδηλώσεις της. Κάθε παιδί ενός προσβεβλημένου γονέα έχει πιθανότητα 50% να κληρονομήσει το ανώμαλο γονίδιο.
Τα γονίδια τα οποία είναι υπεύθυνα για την Αυτοσωματική Επικρατούσα Πολυκυστική Νόσος των Νεφρών (ADPKD) είναι τα PKD1 (χρωμόσωμα 16p13.3) σε ποσοστό 78% και PKD2 (χρωμόσωμα 4q21) σε ποσοστό 13%. Πρόσφατα, τυποποιήθηκαν οικογένειες χωρίς τις παραπάνω γνωστές γονιδιακές μεταλλάξεις σε ποσοστό 9% (δηλαδή αρνητικό οικογενειακό ιστορικό). Αίτια για την απουσία των γνωστών αυτών μεταλλάξεων στα γονίδια PKD1 – PKD2 (και επομένως την απουσία θετικού οικογενειακού ιστορικού) αποτελούν οι νέες (de-novo) μεταλλάξεις, η εικόνα μωσαϊκού, οι μεταλλάξεις μη-αποκοπής στο PKD1 (non-truncating PKD1 mutations) κοκ.
Αυτά τα γονίδια οδηγούν στην παθολογική κωδικοποίηση των πρωτεϊνών πολυκυστίνη 1 και πολυκυστίνη 2. Οι πολυκυστίνες εντοπίζονται στους κροσσούς των σωληναριακών κυττάρων. Η μειωμένη έκφραση αυτών των πρωτεϊνών οδηγεί στην διαταραχή της ομοιόστασης του ενδοκυττάριου ασβεστίου και εν τέλει στην πολυκυστική νόσο των νεφρών και στις εξωνεφρικές εκδηλώσεις της νόσου. Η κληρονόμηση και των δύο αλληλόμορφων γονιδίων PKD1 (ή των δύο αλληλόμορφων PKD2) προκαλεί τον θάνατο ήδη από την εμβρυική ζωή.
Πρόγνωση στην ADPKD
Οι κυστικοί νεφροί συνήθως διατηρούν το σχήμα «φασολιού», με το μέγεθός τους να κυμαίνεται από ελάχιστα έως μέτρια αυξημένο στα πρώιμα στάδια της νόσου, ενώ στο τελικό στάδιο της νόσου είναι συνήθως αρκετές φορές μεγαλύτεροι (μέχρι και 20 φορές) σε σχέση με το αρχικό τους μέγεθος. Έως και το 90% των ασθενών με αυτοσωματική επικρατούσα πολυκυστική νόσος των νεφρών (ADPKD) εμφανίζουν κύστεις και στο ήπαρ. Όσο αφορά την πρόβλεψη της εξέλιξης της νόσου, ο αρχικός συνολικός όγκος των νεφρών αποτελεί έναν καλό δείκτη πρόβλεψης της απώλειας του ρυθμού σπειραματικής διήθησης (GFR) στην διάρκεια του χρόνου (μελέτη CRISP).
Οι ασθενείς με Αυτοσωματική Επικρατούσα Πολυκυστική Νόσος των Νεφρών (ADPKD) που θα καταλήξουν τελικά στην αιμοκάθαρση παρουσιάζουν μικρότερα ποσοστά νοσηρότητας και θνησιμότητας συγκριτικά με ασθενείς που καταλήγουν στην αιμοκάθαρση από άλλα αίτια. Η διαφορά αυτή φαίνεται ότι έχει να κάνει εν μέρη με την αυξημένη παραγωγή της ενδογενούς ερυθροποιητίνης και επομένως την καλύτερη επίτευξη συγκέντρωση αιμοσφαιρίνης.
Διάγνωση στην ADPKD με Θετικό Οικογενειακό Ιστορικό
Η διάγνωση της ADPKD σε ένα άτομο με θετικό οικογενειακό ιστορικό βασίζεται στον απεικονιστικό παρακλινικό έλεγχο, με τον υπέρηχο να αποτελεί την εξέταση εκλογής λόγω του χαμηλού κόστους και της ασφάλειας που παρέχει. Τα υπερηχογραφικά διαγνωστικά κριτήρια για την PKD1 εξαρτώνται από τον αριθμό των κύστεων και την ηλικία του ασθενή. Συγκεκριμένα, η παρουσία τουλάχιστον δύο κύστεων ετερόπλευρων ή αμφοτερόπλευρων θεωρείται επαρκής για τη διάγνωση της νόσου σε άτομα ηλικίας 15 έως 29 και 30-59 ετών αντίστοιχα (με θετικό οικογενειακό ιστορικό). Αντιθέτως, σε άτομα 60 ετών και άνω απαιτούνται τουλάχιστον τέσσερις κύστεις σε κάθε νεφρό (με θετικό οικογενειακό ιστορικό). Αντιθέτως, η παρουσία μίας κύστης σε κάθε νεφρό θεωρείται επαρκής για τον αποκλεισμό της νόσου σε άτομα υψηλού κινδύνου ηλικίας μεγαλύτερης των 30 ετών.
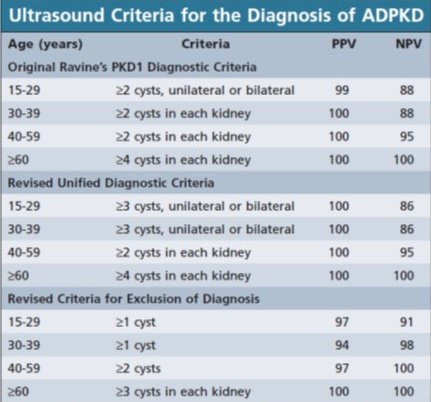
Η παρουσία ενός μέλους στην οικογένεια που κατέληξε στην αιμοκάθαρση μέχρι την ηλικία των 55 ετών (λόγω της ADPKD) έχει 100% θετική προγνωστική αξία για PKD1. Αντιθέτως, ένα οικογενειακό ατομικό αναμνηστικό για την παρουσία μέλους που κατέληξε στην αιμοκάθαρση στην ηλικία των 70 ετών και άνω έχει θετική προγνωστική αξία για PKD2.
Διάγνωση στην ADPKD με Αρνητικό Οικογενειακό Ιστορικό

Γενετικός Έλεγχος και Προεμφυτευτική Γενετική
Πολυκυστική Νόσος των Νεφρών και Λευκωματουρία
Πολυκυστική Νόσος των Νεφρών και Υπέρταση
Η υπέρταση (συστολική αρτηριακή πίεση ≥140mmHg, διαστολική ΑΠ ≥90mmHg) αποτελεί μια αρκετά συχνή και πρώιμη εκδήλωση της ADPKD, η οποία επηρεάζει περίπου το 60% των ασθενών και αυτό πριν από οποιαδήποτε ανιχνεύσιμη διαταραχή της νεφρικής λειτουργίας. Αποτελεί μία πρώιμη εκδήλωση της ADPKD στο 30% των περιπτώσεων. Η μέση ηλικία έναρξης της είναι τα 30 έτη και τείνει να είναι πιο σοβαρή στην PKD1 (σε σχέση με την PKD2). Η επιπολασμός αλλά και η βαρύτητα της υπέρτασης στην ADPKD σχετίζονται με το ρυθμό αύξησης του όγκου των νεφρών στον χρόνο (δηλαδή του αριθμού και του μεγέθους των κύστεων). Η διάγνωση της γίνεται συχνά αργά. Η 24ωρη καταγραφή σε παιδιά ή νεαρούς ενήλικες χωρίς υπέρταση μπορεί να αποκαλύψει διαταραχές στον κιρκάδιο ρυθμό ή διαταραχές κατά την διάρκεια της άσκησης. Επειδή τα καρδιαγγειακά επεισόδια αποτελούν τα κύρια αίτια θανάτου η έγκαιρη διάγνωση και θεραπεία της είναι πολύ σημαντική.
Πολυκυστική Νόσος των Νεφρών και Αιμορραγία
Η αιμορραγία μπορεί να προκληθεί από τραύματα-πλήξη της κοιλιακής χώρας, άσκηση, ρήξη, λοίμωξη του κατώτερου ουροποιητικού συστήματος (κυστίτιδα) ή του ανώτερου ουροποιητικού (πυελονεφρίτιδα), επιπλεγμένη λοίμωξη κύστης, νεφρολιθίαση. Ως εκ τούτου, οι ασθενείς με Αυτοσωματική Επικρατούσα Πολυκυστική Νόσος των Νεφρών (ADPKD) συνίσταται να αποφεύγουν επικίνδυνες και επίπονες ασκήσεις. Εμφανίζεται συχνότερα στους μεγάλους σε μέγεθος νεφρούς και μπορεί να σχετίζεται με αιματουρία και πυρετό, αλλά συχνά ο εντοπισμένος πόνος είναι το μόνο σύμπτωμα κατά την παρουσίαση. Η θεραπεία μιας απλής αιμορραγικής κύστης περιλαμβάνει ενυδάτωση, ξεκούραση, παυσίπονα και αποχή από την αντί-υπερτασική αγωγή έως ότου επιλυθεί το οξύ επεισόδιο. Οι περισσότερες αιμορραγίες συνήθως αυτοπεριορίζονται και υποχωρούν μέσα σε 7 ημέρες.
Πολυκυστική Νόσος των Νεφρών και Νεφρική Λειτουργία
Η εξέλιξη της νεφρικής ανεπάρκειας στην ADPKD παρουσιάζει μεγάλες διακυμάνσεις, με τους περισσότερους ασθενείς να διατηρούν
Ωστόσο, ένας από τους ισχυρότερους προγνωστικούς παράγοντες εξέλιξης της νεφρικής ανεπάρκειας (και μείωσης του GFR) παραμένει ο όγκος των νεφρών και των κύστεων σύμφωνα με την μελέτη CRISP.
Πολυκυστική Νόσος των Νεφρών και Νεφρολιθίαση

Εξωνεφρικές Εκδηλώσεις
Η Πολυκυστική ηπατική νόσος (PLD) είναι η πιο κοινή εξωνεφρική εκδήλωση της ADPKD και σχετίζεται τόσο με την PKD1 όσο και με την PKD2. 
Η PLD είναι συνήθως ασυμπτωματική και δεν χρήζει συνήθως θεραπεία. Αποφυγή ηπατοτοξικών φαρμάκων, αλκοόλ και καφεΐνης είναι κάποιες από τις γενικές οδηγίες που δίνονται στους ασθενείς. Άλλες εκδηλώσεις της ADPKD περιλαμβάνουν τα ανευρύσματα (ενδοκρανιακά, στεφανιαία), καθώς και τον διαχωρισμό της θωρακικής αορτής. Τα ενδοκρανιακά ανευρύσματα συμβαίνουν σε περίπου 6% – 8% των ασθενών με αρνητικό οικογενειακό ιστορικό και στο 16% των ατόμων με θετικό οικογενειακό ιστορικό ανευρυσμάτων. Συνήθως είναι ασυμπτωματικά με τη μέση ηλικία των ασθενών κατά την ρήξη να είναι χαμηλότερη από αυτή του γενικού πληθυσμού (39 έτη έναντι 51 έτη αντίστοιχα). Η πρόπτωση της μιτροειδούς, η ανεπάρκεια της αορτικής βαλβίδας, οι βρογχεκτασίες και τα εκκολπώματα αποτελούν επίσης εξωνεφρικές εκδηλώσεις της ADPKD.
Θεραπεία της ADPKD

Οι αναστολείς του συστήματος mTOR (everolimus, sirolimus – rapamycin) αποτελούν ένα μονοπάτι στην θεραπευτική προσέγγιση της νόσου. Ωστόσο, τα αντικρουόμενα αποτελέσματα των μελετών (κυρίως για τον ρυθμό απώλειας της νεφρικής λειτουργίας) και η διαπίστωση ότι το sirolimus – rapamycin ήταν αναποτελεσματικό και όχι ασφαλές σε ασθενείς με ADPKD και νεφρική ανεπάρκεια (Sirena-2 μελέτη), έχουν μετριάσει τον αρχικό ενθουσιασμό που υπήρχε για την χρησιμοποίησή αυτών των φαρμάκων.
Η επίδραση της βασοπρεσσίνης, μέσω των υποδοχέων V2 στα αθροιστικά σωληνάρια (το κύριο μέρος ανάπτυξης των κύστεων στην αυτοσωματική επικρατούσα πολυκυστική νόσος των νεφρών), αποτέλεσε το κύριο ερέθισμα για την ανάπτυξη μελετών που θα αναδείκνυαν την αποτελεσματικότητα των ανταγωνιστών αυτής.
Τολβαπτάνη και ADPKD
Πρόσφατα, ο Ευρωπαϊκός Οργανισμός Φαρμάκων (2015), ενέκρινε τη χρήση της τολβαπτάνης (ανταγωνιστής V2 των υποδοχέων της βασοπρεσσίνης) για να επιβραδύνει την εξέλιξη της ανάπτυξης των κύστεων και της νεφρικής ανεπάρκειας στην ADPKD σε ενήλικες ασθενείς με νεφρική ανεπάρκεια σταδίου I – III (GFR≥30 mL/min/1.73 m²) και με ενδείξεις ταχέως εξελισσόμενης νόσου. Στη μελέτη TEMPO 3:4 και 4:4 ασθενείς με ADPKD και ταχεία εξέλιξη της νόσου με συνολικό όγκο νεφρών τουλάχιστον 750 mL, ηλικίας μεταξύ 18 και 50 ετών και νεφρική ανεπάρκεια σταδίου I – IIIb (GFR≥30 mL/min/1.73 m²) έλαβαν την τολβαπτάνη για 3 έτη. Οι ασθενείς αυτοί επιβράδυναν τον ρυθμό αύξησης του όγκου των νεφρών κατά 49% και την απώλεια της νεφρικής λειτουργίας κατά 26% ανά έτος και μείωσαν την συχνότητα κλινικών εκδηλώσεων της νόσου (ουρολοιμώξεις, αιμορραγίες, πόνος κοκ) κατά την διάρκεια παρακολούθησης των τριών αυτών ετών.
Αλλά και για ασθενείς με νεφρική ανεπάρκεια σοβαρότερου βαθμού, σταδίου IV και GFR≥25 mL/min/1.73 m², η μελέτη REPRISE έδειξε το ίδιο καλά αποτελέσματα όσο αφορά το ρυθμό αύξησης του όγκου των νεφρών και της απώλειας της νεφρικής λειτουργίας. Στα αποτελέσματα αυτής της μελέτης στηρίχθηκε ο Αμερικανικός Οργανισμός Φαρμάκων (2018) και ενέκρινε την χρήση της τολβαπτάνης για την πολυκυστική νόσο των νεφρών.
Ωστόσο, λόγω των ανεπιθύμητων παρενεργειών του φάρμακου που σχετίζονται με την αποβολή ύδατος (πολυουρία, νυκτουρία, συχνουρία, δίψα, αύξηση του νατρίου και του ουρικού στον ορό του αίματος), αλλά και την αύξηση των ηπατικών ενζύμων (ηπατοτοξικότητα), ο νεφρολόγος πρέπει να είναι πολύ προσεκτικός και να ακολουθεί τις συστάσεις για την χρήση της τολβαπτάνης στην ADPKD (ERA-EDTA Working Groups on Inherited Kidney Disorders and European Renal Best Practice).
Ποια ποσότητα νερού είναι ασφαλής και κατάλληλη στην ADPKD;
Στα πλαίσια πρόληψης για την ταχύτητα εξέλιξης της νόσου η αυξημένη πρόσληψη νερού (καταστέλλει τα επίπεδα βασοπρεσσίνης) σε ασθενείς με νεφρική ανεπάρκεια σταδίου III, τόσο ώστε να επιτευχθεί μία ωσμωτικότητα ούρων ίση – μικρότερη από τα 260 mOsm/kg H2O, φαίνεται εν μέρει να το επιτυγχάνει. Αν υποθέσουμε ότι το άθροισμα των τελικών προϊόντων του μεταβολισμού που εκκρίνονται με τα ούρα την ημέρα είναι κατά μέσο όρο 800 mOsm στην γυναίκα και 1100 mOsm στον άνδρα, ο ελάχιστος όγκος ούρων που απαιτείται είναι 2.8 και 3.7 Lt / ημέρα αντίστοιχα. Έτσι, μια ημερήσια πρόσληψη νερού περίπου 3Lt για τις γυναίκες και 4Lt για τους άνδρες σε εύκρατα κλίματα θα ήταν επαρκής για να μειώσει την συγκέντρωση της βασοπρεσσίνης (AVP<2.5 pg/ml) στο πλάσμα στα επιθυμητά όρια (αντίστοιχα της μελέτης TEMPO).